AcuCort AB (”AcuCort” eller ”Bolaget”) publicerade den 28 april 2026 Bolagets delårsrapport för det första kvartalet år 2026. Följande är några punkter som vi valt att belysa i samband med rapporten:
- Kommersiellt femårigt genombrottsavtal med Glenmark Pharmaceuticals — marknadsexponering ökar till ca 200 miljoner invånare
- Överenskommelse med FDA avseende iPSP — ingen pediatrisk studie krävs före NDA-inlämning
- Stärkt momentum i partnerpipen — 44 möten på Bio Europe Spring och flera ingångna sekretessavtal
- Disciplinerad kostnadskontroll trots ökad intensitet i kommersialiseringen — OPEX om ca 6,8 MSEK (5,9), +16,6 % Y-Y
- Kassa om ca 21,2 MSEK — estimerad finansieringshorisont till Q1-27
- SBW-besked, NDA-inlämning, Glenmarks marknadsansökningar samt nya avtal utgör centrala triggers att bevaka under år 2026
Genombrottsavtal med Glenmark Pharmaceuticals
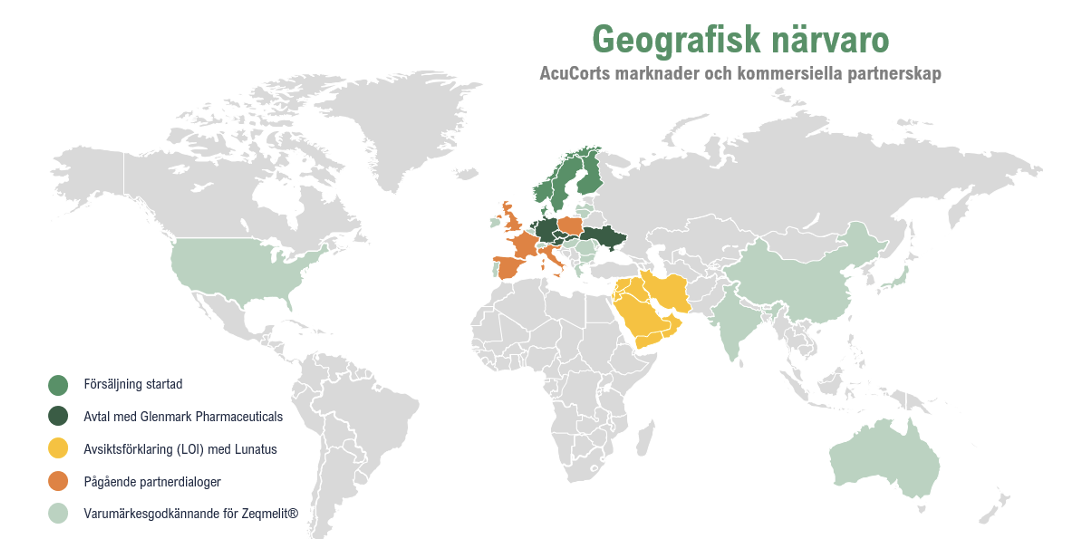
Glenmark Pharmaceuticals, ett av världens 100 största bioläkemedelsbolag med verksamhet i över 80 länder, valde under inledningen av år 2026 att ingå ett kommersiellt femårigt avtal med AcuCort avseende marknadsföring och distribution av Zeqmelit®, vilket utgör en strategisk milstolpe som inte bara breddar Bolagets geografiska räckvidd utan även stärker dess attraktivitet i pågående och framtida partnerdialoger. Avtalet täcker Tyskland, Nederländerna, Tjeckien, Österrike, Slovakien och Ukraina, marknader med en samlad befolkningsbas om ca 200 miljoner invånare, motsvarande ca 7x den nordiska hemmamarknaden.
Avtalet är strukturerat som en trappstegsmodell med årligt ökande minimiåtaganden från Glenmark, i kombination med årliga investeringsåtaganden från partnerns sida. Att Glenmark accepterat en sådan struktur signalerar en stark tilltro till Zeqmelits® potential, och talar för en gradvis försäljningsökning i takt med att Glenmark rullar ut läkemedlet på ovan nämnda marknader. Vidare agerar Glenmark Market Authorisation Holder (MAH), och därmed bär det regulatoriska ansvaret i respektive marknad, vilket både reducerar AcuCorts regulatoriska riskexponering samt medför minskade kostnader. De första marknadsansökningarna förväntas skickas in under Q4-26 via Repeat Use Procedure (RUP), vilket innebär att en redan genomförd MRP-process återanvänds för att utvidga godkännandet till ytterligare EU-medlemsstater, en regulatoriskt effektiv väg som drar fördel av de tidigare nordiska godkännandena. Givet sedvanliga handläggningstider estimerar Analyst Group en potentiell intäktsstart under H2-27, där Tyskland förväntas vara först ut, vilket är logiskt givet marknadens storlek och dess roll som referens för efterföljande lanseringar.
Regulatorisk framdrift i USA öppnar vägen för NDA-inlämning under år 2026
Efter periodens utgång meddelade AcuCort att Bolaget nått en överenskommelse med FDA avseende den Initial Pediatric Study Plan (iPSP) som inlämnades under Q4-24. Innebörden är att FDA accepterat att inga ytterligare kliniska studier (pediatriska) krävs före inlämnandet av en NDA-ansökan i USA. Detta eliminerar en central osäkerhetsfaktor som länge präglat den amerikanska processen, såväl tidsmässigt som kostnadsmässigt, och reducerar den regulatoriska risken väsentligt. Vägen mot en NDA-ansökan via en 505(b)(2)-procedur under innevarande år ligger därmed öppen, i linje med Bolagets kommunicerade målsättning.
Det enda kvarvarande steget före NDA-inlämning är en förnyelse av Bolagets Small Business Waiver (SBW), som vid godkännande befriar AcuCort från ansökningsavgiften om ca 16 MSEK. Givet att Bolaget fortsatt kvalificeras som ett mindre bolag bedöms SBW-förnyelsen vara en administrativ formalitet, i synnerhet då myndigheten har godkänt den två gånger tidigare. AcuCort inväntar besked från FDA före sommaren, vilket banar väg för en NDA-inlämning under innevarande år. Vid en sedvanlig handläggningstid om ca 12 månader för en 505(b)(2)-procedur kvarstår vår bedömning om ett potentiellt FDA-godkännande och försäljningsstart under år 2027.
AcuCort avser nå den amerikanska marknaden via en licensmodell, där varje regulatoriskt framsteg stärker Bolagets förhandlingsläge gentemot potentiella licenspartners. I kombination med Glenmark-avtalet förhandlar AcuCort nu från en fundamentalt annorlunda position än för ett år sedan, vilket bedöms skapa förutsättningar för mer fördelaktiga licensvillkor avseende såväl upfront-betalningar, milstolpsbetalningar som royalty rate.
Bredare partnerpipeline validerar Zeqmelit® som internationellt gångbar produkt
Glenmark-avtalet och FDA-framstegen har även en indirekt effekt på AcuCorts övriga partnerprocesser. Det konkreta genomslaget syns i partnerpipen. Under Q1-26 medverkade AcuCort på Bio Europe Spring i Lissabon, där Bolaget i en efterföljande intervju betonade att 44 möten genomfördes, varav ca 90 % utgjordes av nya kontakter med en geografiskt bred spridning över Europa, Asien och USA, och 15 motparter var beredda att teckna sekretessavtal på plats. I samband med presentationen av Q1-rapporten lyfter AcuCort därtill att flera sekretessavtal nu har ingåtts, vilket bekräftar att momentumet i partnerpipen har konkret bäring.
En central observation från dessa dialoger är att flera potentiella partners uttryckt intresse för Zeqmelits® bredare indikationsspektrum, utöver den primära allergi-indikationen är produkten godkänd för bl.a. akut svår astma, krupp, illamående vid cytostatikabehandling samt akuta hudsjukdomar, vilket utgjort en betydelsefull faktor i kommersiella diskussioner. Detta indikerar att den kommersiella potentialen i Zeqmelit® inte är begränsad till en enskild indikationsmarknad, utan att den underliggande affärsmöjligheten är bredare än vad det initiala allergi-fokuset signalerar. Under sommaren år 2026 avser Bolaget medverka på BIO International Convention i San Diego, följt av BIO-Europe i Köln under Q4-26, vilka bedöms utgöra strategiskt välplacerade arenor för dialoger med potentiella partners, i synnerhet amerikanska licenspartners inför en stundande NDA-inlämning.
Vad gäller LOI:t med Lunatus avseende Mellanöstern och Gulfregionen har förhandlingarna tagit längre tid än inledningsvis estimerat, primärt till följd av komplexiteten i att identifiera rätt affärsstruktur för regionen. Samtidigt har AcuCort mottagit flera parallella förfrågningar från regionen, vilket föranlett Bolaget att konkurrensutsätta Lunatus, ett strategiskt val som bedöms stärka förhandlingspositionen och indikerar att det strategiska värdet av Mellanöstern-exponeringen består oavsett utfallet med just Lunatus. Dialoger fortsätter även på prioriterade marknader såsom Storbritannien, Frankrike och Polen, vilket sammantaget signalerar att den kommersiella aktiviteten är hög, och flera potentiella avtal utgör triggers att bevaka under resterande år 2026.
Kostnadsmedveten uppbyggnad i takt med intensifierad kommersialiseringsfas
Ingen nettoomsättning har rapporterats under Q1-26. Detta är förenligt med Bolagets kommunikation om att den fjärde ordern från Unimedic Pharma om ca 1,2 MSEK levereras under maj 2026 och därmed väntas redovisas som omsättning under Q2-26.
Rörelsekostnaderna (exkl. avskrivningar) uppgick till ca 6,8 MSEK (5,9), motsvarande en ökning om 16,6 % Y-Y, varav personalkostnaderna ökade till ca 1,7 MSEK (1,2) primärt till följd av att Anna Chérouvrier Hansson tillträdde som Business Development Director under Q4-25, medan övriga externa kostnader uppgick till ca 5,1 MSEK (4,7). De totala kostnaderna har under perioden utfallit lägre än prognos, vilket Analyst Group bedömer som en signal om disciplinerad kostnadskontroll trots den intensifierade kommersialiseringsfasen. Etableringen av ett farmakovigilanssystem i egen regi understödjer denna utveckling, då initiativet minskar beroendet av externa konsulter och bidrar till en mer kostnadseffektiv struktur över tid. Aktiverade utvecklingsutgifter om ca 2,2 MSEK (1,4) är främst hänförliga till stabilitetsstudier, det regulatoriska arbetet i USA samt vidareutveckling av produktionsprocessen.
Vid utgången av Q1-26 uppgick kassan till ca 21,2 MSEK. Den genomsnittliga operativa kapitalförbrukningen uppgick till ca 1,2 MSEK/mån, en tydlig förbättring Y-Y samt Q-Q, då den uppgick till 2,1 MSEK/mån respektive 1,8 MSEK/mån. Inklusive investeringar uppgick det negativa fria kassaflödet till ca 2,0 MSEK/mån, vilket även det utgör en förbättring såväl på årsbasis som sekventiellt
Med en estimerad kapitalförbrukning om ca 2 MSEK/mån framgent estimeras Bolaget vara finansierat till inledningen av Q1-27, allt annat lika. En avgiftsbefriad NDA-ansökan genom SBW, i kombination med Glenmarks regulatoriska åtaganden, reducerar därtill det framtida kapitalbehovet. Analyst Group bedömer att AcuCort därmed befinner sig i ett finansiellt handlingsläge som möjliggör ett selektivt förhållningssätt i partnerförhandlingar, en viktig position inför en period med flera parallella licens- och distributionsdialoger.
Sammanfattningsvis bedömer Analyst Group att AcuCort under Q1-26 har förflyttat sig från en nordisk kommersiell etablering till en bredare internationell positionering, drivet av genombrottsavtalet med Glenmark Pharmaceuticals och den efterföljande FDA-överenskommelsen avseende iPSP:n. Glenmark-avtalet, som breddar Bolagets marknadsexponering till ca 200 miljoner invånare, bedöms fungera som en extern kvalitetsstämpel inför pågående och kommande partnerdialoger, samtidigt som FDA-beskedet banar väg för en NDA-inlämning under innevarande år. På den nordiska hemmamarknaden inleds samtidigt allergisäsongen, vilket historiskt sammanfaller med ökad förskrivningsaktivitet och kan ge utrymme för större ordrar från Unimedic Pharma framgent. Centrala triggers att bevaka framgent inkluderar en beviljad SBW, efterföljande NDA-inlämning, Glenmarks marknadsansökningar under Q4-26, konvertering av LOI:t med Lunatus samt nya partneravtal, där medverkan på BIO International Convention i juni 2026 bedöms kunna fungera som en katalysator för flera av dessa processer.
Vi kommer att återkomma med en uppdaterad aktieanalys av AcuCort.





