DexTech Medical AB (”DexTech” eller ”Bolaget”) meddelade den 16 oktober år 2025 att dosgrupp 2 (6 mg/kg) i den pågående fas I-studien avseende läkemedelskandidaten OsteoDex inom multipelt myelom (MM) nu är färdigrekryterad, och att de sista två patienterna förväntas vara färdigbehandlade i början av december. Vidare har den oberoende datamonitoreringskommittén (DMC) godkänt att Bolaget går vidare till dosgrupp 3, då inga OsteoDex-relaterade allvarliga biverkningar har noterats. En ny patient för dosgrupp 3 har screenats.
Analyst Groups syn på uppdateringen
DMCs Beslut att gå vidare till dosgrupp 3 konfirmerar ytterligare OsteoDex höga tolererbarhet med frånvaro av allvarliga biverkningar, vilket utgör den primära målsättningen i fas I-studien. Godkännandet från DMC att fortsätta till dosgrupp 3, i kombination med att dosgrupp 2 nu är färdigrekryterad, visar att DexTech fortsätter att ta steg framåt i den kliniska utvecklingen av OsteoDex.
Det är samtidigt viktigt att beakta att studien omfattar svårt sjuka patienter med behandlingsresistent och progredierande cancer som genomgått flera tidigare behandlingslinjer (1–5). Givet patienternas sköra hälsotillstånd finns en inneboende osäkerhet kopplad till studiens rekryteringstakt och genomförande, då faktorer såsom sjukdomsprogress eller dödsfall kan påverka tidsplanen. Dagens besked indikerar emellertid att studien fortlöper väl och att DexTech tar steg i riktning mot att slutföra doseskaleringen.
Framgent bedömer vi att slutförandet av fas I-studien utgör en viktig trigger, vilken vid goda resultat kan bidra till att reducera den kliniska risken och öka värdet på Bolagets forskningsportfölj. Den mest centrala värdedrivaren för att realisera portföljens potential är dock fortsatt ingåendet av ett potentiellt licensavtal avseende OsteoDex – där DexTech framstår som en alltmer attraktiv partner ju längre det kliniska arbetet fortlöper.
Fas I-studien (multipelt myelom)
Den pågående fas I-studien inleddes i mars år 2023, och genomförs vid Karolinska Universitetssjukhuset Huddinge och Uddevalla Sjukhus under ledning av Dr Katarina Uttervall respektive Dr Dorota Knut. Studien omfattar 12 patienter med recidiverande eller behandlingsresistent multipelt myelom som tidigare genomgått 1–5 behandlingslinjer. Patienterna delas in i tre dosgrupper (3, 6 och 9 mg/kg) med fyra patienter per grupp, där behandlingen ges varannan vecka under totalt 14 veckor.
Resultaten från den första dosgruppen (3 mg/kg) presenterade under april år 2025, vilka var mycket lovande – samtliga patienter uppvisade stabil sjukdom utan allvarliga biverkningar. Vid uppföljning utan ytterligare cancerbehandling varierade tid till sjukdomsprogress mellan 39-188 dagar, vilket är jämförbart med etablerade läkemedel som ges fortlöpande fram till resistens. Detta indikerar att OsteoDex kan ge en bestående sjukdomsbromsande effekt även efter avslutad behandling.
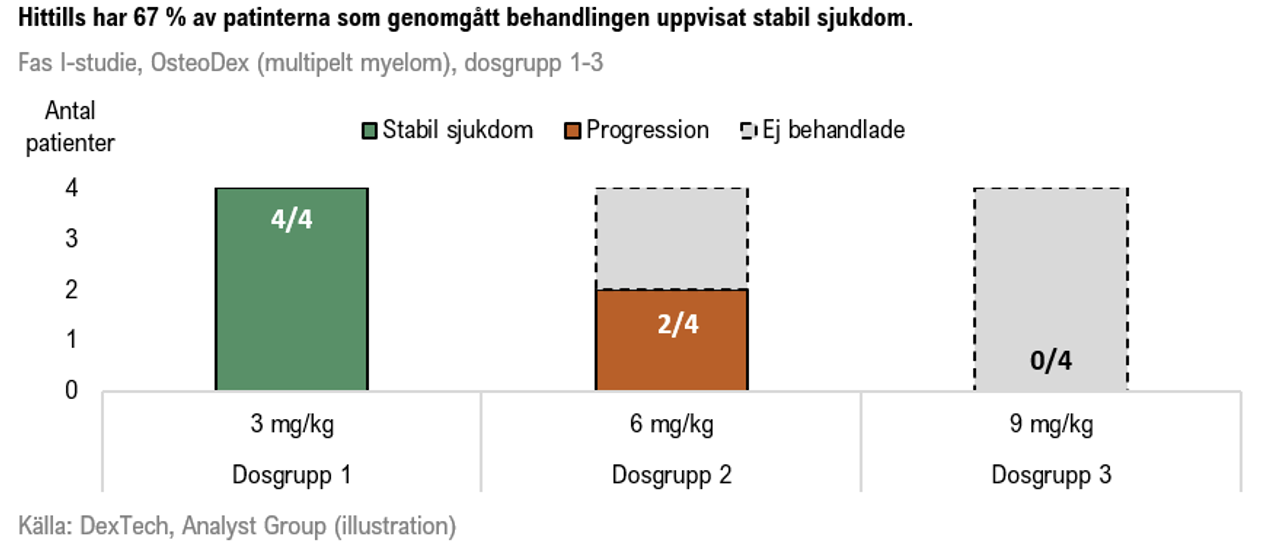
I augusti år 2025 rapporterades att två patienter i dosgrupp 2 (6 mg/kg) hade genomgått behandling och därefter utvecklat progressiv sjukdom. Den 16 oktober år 2025 meddelade DexTech att dosgrupp 2 nu är färdigrekryterad, och att de sista två patienterna förväntas vara färdigbehandlade i början av december. Vidare meddelade Bolaget att den oberoende datamonitoreringskommittén (DMC) godkänt att studien fortsätter till dosgrupp 3 (9 mg/kg), baserat på att inga OsteoDex-relaterade allvarliga biverkningar har observerats. En ny patient för den högsta dosgruppen har redan screenats.
Sammanfattningsvis bedömer Analyst Group att DMC:s godkännande att avancera till dosgrupp 3 bekräftar OsteoDex goda säkerhetsprofil och visar på fortsatt klinisk progression. Att dosgrupp 2 nu är färdigrekryterad indikerar att studien fortlöper enligt plan. Tidsplanen kan påverkas av patienternas sköra hälsotillstånd och därmed medföra förskjutningar i tidsplanen. Slutförandet av fas I-studien utgör en central värdedrivande milstolpe framgent, där positiva data kan minska den kliniska risken och stärka DexTechs förhandlingsposition i potentiella licensdiskussioner.




